Теплоемкость идеального газа
Определение теплоемкости
![]()
называется теплоемкостью.
Теплоемкость – это количество тепла, которое затрачивается для того, чтобы повысить температуру тела на один кельвин. Теплоемкость зависит от массы вещества, условий при которых системе сообщают теплоту. Уравнение (1) – это определение теплоемкости через интегральные параметры. Иногда удобнее использовать следующее определение теплоемкости:
![]()
где ![]() – бесконечно мало количество плоты, которое получает тело; dT – приращение температуры тела.
– бесконечно мало количество плоты, которое получает тело; dT – приращение температуры тела.
При единичной массе тела теплоемкость называют удельной. Обозначают ее обычно маленькой буквой c. Еще используют молярную теплоемкость (![]() ) – это теплоемкость одного моля вещества.
) – это теплоемкость одного моля вещества.
Теплоемкость и первое начало термодинамики
Используя первое начало термодинамики в интегральной записи, теплоёмкость можно найти как:
![]()
где ![]() – изменение внутренней энергии термодинамической системы; A – работа системы над внешними силами. Для идеального газа имеем:
– изменение внутренней энергии термодинамической системы; A – работа системы над внешними силами. Для идеального газа имеем:
![]()
где m – масса газа; ![]() – молярная масса газа; R – универсальная газовая постоянная.
– молярная масса газа; R – универсальная газовая постоянная.
В дифференциальном виде:
![]()
Для идеального газа теплоемкость равна:
![Rendered by QuickLaTeX.com \[C=\frac{\frac{i}{2}\frac{m}{\mu}RdT+pdV}{dT}=\frac{i}{2}\frac{m}{\mu}R+p\frac{dV}{dT} \qquad (6) \]](http://ru.solverbook.com/wp-content/ql-cache/quicklatex.com-bc49437affd37c7a2b86038ef2b410a7_l3.png)
Теплоемкость для процессов, проводимых в идеальном газе
Теплоемкость связана с характером процесса. Она может изменяться от бесконечных отрицательных величин до бесконечных положительных.
Рассмотрим изохорный процесс ![]() . При проведении изохорного процесса газ работы не совершает, поэтому теплоемкость газа в изохорном процессе (
. При проведении изохорного процесса газ работы не совершает, поэтому теплоемкость газа в изохорном процессе (![]() ) равна:
) равна:
![]()
Или:
![]()
При изобарном процессе (![]() ) теплоемкость обозначают как
) теплоемкость обозначают как ![]() . Она равна:
. Она равна:
![]()
Или:
![]()
Теплоемкости, при постоянных давлении и объеме, являются функциями состояний. Надо отметить, что независимость теплоемкости от температуры не подтвердили эксперименты.
В изотермическом процессе теплоемкость идеального газа считают бесконечной:
![]()
В адиабатном процессе теплоемкость равна нулю.
Примеры решения задач
| Задание | На рис. 1 изображен график процесса АВ с постоянной массой идеального газа. Кривая, изображенная на рисунке – изотерма. Сравните теплоемкость в процессе АВ с теплоемкостью в этой же массы газа в изохорном процессе.
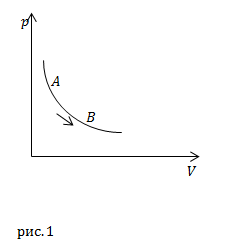
|
| Решение | Теплоемкость при изохорном процессе в идеальном газе вычисляется при помощи формулы:
Для постоянной массы одного и того же газа она величина постоянная. По условию задачи с газом проводят изотермический процесс. В изотермическом процессе теплоемкость бесконечна. Получается, что в процессе АВ теплоёмкость больше. |
| Ответ |
| Задание | Каким будет знак молярной теплоемкости идеального газа в процессе: |
| Решение | У трехатомных жестких молекул число степеней свободы равно шести ( Уравнение процесса В таком случае: Давление выразим из уравнения состояния идеального газа: Подставим (2.3) и (2.4) в (2.1), имеем: При |
| Ответ |











