Тип кристаллической решетки алюминия
Для решения задачи, мне нужно указать тип кристаллической решетки алюминия. Буду очень признателен тому, кто поможет мне в этом деле. А еще, нужны способы получения алюминия.
Отображением пространственной структуры монокристалла служит его кристаллическая решетка. Таким образом, различие геометрических форм кристаллов тех или иных веществ связано с особенностями симметрии их кристаллических решеток. Обычно оценивают следующие элементы симметрии в монокристалле: оси симметрии, плоскости симметрии и центры симметрии. Если при повороте на определенный угол вокруг воображаемой оси кристаллическая решетка совмещается сама с собой, то это свидетельствует о наличии в кристалле оси симметрии. Если в кристалле можно провести одну или несколько плоскостей таким образом, что одна часть кристаллической решетки будет зеркальным отображением другой, значит в кристалле имеются плоскости симметрии. Наконец, когда отражение всех узлов решетки в какой-либо точке кристалла приводит к их совмещению, говорят о существовании центра симметрии.
Кристаллическая решетка представляет собой своего рода пространственный каркас, образованный пересекающимися прямыми линиями. В точках пересечения линий – узлах решетки – лежат центры частиц.
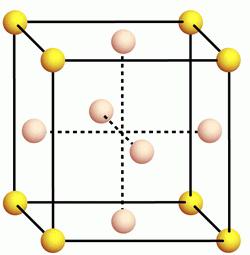
Тип кристаллической решетки алюминия — молекулярная гранецентрированная кубическая. Это означает, что в её узлах находятся молекулы. Они связаны друг с другом межмолекулярными силами.
Алюминий – металл, относится к элементам p-семейства. Электронная конфигурация алюминия выглядит следующим образом:
![]() .
.
На внешнем энергетическом уровне алюминия находится 3 электрона, из которых один неспаренный. Два из вышеуказанных валентных электронов находятся на s-орбитали, а один – на p-орбитали. s- и p-уровни в изолированных атомах близки. Это означает, что соответствующие зоны в кристаллах алюминия перекрываются. Следовательно, число валентных электронов недостаточно для заполнения энергетических уровней перекрывающихся зон.
Таким образом, металлические кристаллы образуются элементами, в атомах которых число валентных электронов мало по сравнению, с числом энергетически близких валентных орбиталей. Вследствие этого химическая связь в металлических кристаллах сильно делокализована.










