Расставьте коэффициенты методом электронного баланса NH3 + O2
Закончите уравнение реакции сгорания аммиака в кислороде. Расставьте коэффициенты методом электронного баланса NH3 + O2 = ? Укажите окислитель и восстановитель.
Окислительно-восстановительными называются такие реакции в результате которых изменяется степень окисления одного или нескольких элементов, входящих в состав реагирующих веществ. Отдача атомом электронов, сопровождающаяся повышением его степени окисления, называется окислением, присоединение атомом электронов, приводящее к понижению его степени окисления, называются восстановлением.
При составлении уравнений ОВР рекомендуется придерживаться следующего порядка:
- составить схему реакции с указанием исходных и образующихся веществ, отметить элементы, изменяющие в результате реакции степень окисления, найти окислитель и восстановитель.
- Составить схему полуреакций окисления и восстановления с указанием исходных и образующихся реально существующих в условиях реакции ионов или молекул.
- Уравнять число атомов каждого элемента в левой и правой частях полуреакций; при этом следует помнить, что в водных растворах могут участвовать ионы
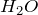 , ионы
, ионы 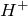 или
или 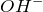 .
. - Уравнять суммарное число зарядов в обеих частях каждой полуреакции; для этого прибавить к левой и правой частям полуреакции необходимое число электронов.
- Подобрать множители (основные коэффициенты) для полуреакций так, чтобы число электронов, отдаваемых при окислении, было равно числу электронов, принимаемых при восстановлении.
- Сложить уравнения полуреакций с учетом найденных основных коэффициентов.
- Расставить коэффициенты в уравнении.
В результате сгорания аммиака в кислороде (NH3 + O2 = ?) происходит образование азота и воды. Молекулярное уравнение реакции имеет вид:
![]()
Химические элементы азот и изменяют свои степени окисления. Схемы электронного баланса выглядят следующим образом:
![]()
![]()










