Порядковый номер фосфора
Каков порядковый номер фосфора в таблице Менделеева? Какие данные можно почерпнуть, зная порядковый номер химического элемента? На чем основан принцип последовательного заполнения орбиталей электронами? Должно ли выполняться какое-то ещё правило помимо принципа Паули?
Порядковый номер фосфора в Периодической таблице – 15. Это означает, что заряд ядра атома фосфора равен +15, внутри ядра находится 15 протонов, а по орбитам вокруг ядра движутся 15 электронов.
Принцип последовательного заполнения орбиталей с наинизшей энергией — группа правил, которые должны выполняться при заполнении электронами атомных или молекулярных орбиталей.
Принцип последовательного заполнения наинизших орбиталей используется в сочетании с двумя другими — правилом Хунда и принципом Паули. Они могут быть суммированы следующим образом:
- Орбитали заполняются, начиная с имеющих самую низкую энергию.
- Если имеется набор вырожденных орбиталей, спаривание электронов на орбитали невозможно до тех пор, пока каждая орбиталь не будет содержать один электрон. Одиночные электроны, занимающие набор вырожденных орбиталей, имеют одинаковые (параллельные) спины. Это правило Хунда.
- Согласно принципу Паули, два электрона в атоме не могут иметь одинаковый набор значений квантовых чисел n, l, m и
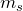 . Это означает, что каждая орбиталь может нести максимум два электрона с различными значениями
. Это означает, что каждая орбиталь может нести максимум два электрона с различными значениями 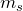 (различными спинами).
(различными спинами).
Первое из приведенных выше утверждений не требует дальнейшего разъяснения. Второе утверждение может быть проиллюстрировано на примере двух электронов, занимающих несколько вырожденных p-орбиталей. Электроны могут быть обозначены стрелочками, ориентация которых показывает направление спина (![]() = +1/2 или -1/2).
= +1/2 или -1/2).
Принцип Паули запрещает двум электронам с одинаковыми спинами занимать одну орбиталь, ведь тогда они имели бы одинаковый набор из четырех квантовых чисел.










